Comparison of rubella seroepidemiology in 17 countries: progress towards international disease control targets
- PMID: 18297166
- PMCID: PMC2647372
- DOI: 10.2471/blt.07.042010
Comparison of rubella seroepidemiology in 17 countries: progress towards international disease control targets
Abstract
Objective: To standardize serological surveillance to compare rubella susceptibility in Australia and 16 European countries, and measure progress towards international disease-control targets.
Methods: Between 1996 and 2004, representative serum banks were established in 17 countries by collecting residual sera or community sampling. Serum banks were tested in each country and assay results were standardized. With a questionnaire, we collected information on current and past rubella vaccination programmes in each country. The percentage of seronegative (< 4 IU/ml) children (2-14 years of age) was used to evaluate rubella susceptibility, and countries were classified by seronegativity as group I (< 5%), group II (5-10%) or group III (> 10%). The proportion of women of childbearing age without rubella protection (< or = 10 IU/ml) was calculated and compared with WHO targets of < 5%.
Findings: Only Romania had no rubella immunization programme at the time of the survey; the remaining countries had a two-dose childhood schedule using the measles, mumps and rubella (MMR) vaccine. The percentage of susceptible children defined five countries as group I, seven as group II and four as group III. Women of childbearing age without rubella protection were < 5% in only five countries.
Conclusion: Despite the low reported incidence in many countries, strengthening the coverage of the routine two-dose of MMR vaccine among children is needed, especially in group III countries. Catch-up campaigns in older age groups and selective targeting of older females are needed in many countries to ensure necessary levels of protective immunity among women of childbearing age.
Objectif: Standardiser la surveillance de la rubéole afin de pouvoir comparer la sensibilité à cette maladie entre l’Australie et 16 pays européens et mesurer les progrès vers les objectifs internationaux de lutte antirubéoleuse.
Méthodes: Entre 1996 et 2004, des banques de sérums représentatifs ont été mises en place dans 17 pays en collectant des résidus de sérum ou en réalisant des prélèvements dans les communautés. Ces banques de sérum ont fait l’objet d’analyses dans chaque pays et les résultats de ces analyses ont été standardisés. Au moyen d’un questionnaire, nous avons collecté des informations sur la situation antérieure et actuelle des programmes de vaccination antirubéoleuse de chaque pays. Le pourcentage d’enfants (2-14 ans) séronégatifs (< 4 UI/ml) a été utilisé pour évaluer la sensibilité à la rubéole et les pays ont été classés par niveau de séronégativité en 3 groupes : I (< 5%), II (5-10%) et III (> 10%). La proportion de femmes en âge de procréer sans protection contre la rubéole (≤ 10 UI/ml) a été déterminée et comparée à l’objectif fixé par l’OMS (< 5%).
Résultats: Seule la Roumanie n’avait pas de programme de vaccination lors de l’enquête, les autres pays appliquant un calendrier de vaccination durant l’enfance par deux doses de vaccin antirougeoleux-antiourlien-antirubéoleux (ROR). D’après le pourcentage d’enfants sensibles, cinq pays ont été classés dans le groupe I, sept dans le groupe II et quatre dans le groupe III. La proportion de femmes en âge de procréer non protégées contre la rubéole était inférieure à 5% dans cinq pays seulement.
Conclusion: Malgré la faible incidence signalée dans de nombreux pays, il faut renforcer la couverture par la vaccination systématique en 2 doses de ROR chez l’enfant, et notamment dans les pays du groupe III. Des campagnes de rattrapage visant les tranches d’âge supérieures et une vaccination sélective des femmes plus âgées s’imposent également dans nombre de pays pour garantir les niveaux d’immunité protectrice nécessaires chez les femmes en âge de procréer.
Objetivo: Normalizar la vigilancia serológica para comparar la vulnerabilidad a la rubéola en Australia y en 16 países europeos, y medir los progresos hacia las metas internacionales de control de esa enfermedad.
Métodos: Entre 1996 y 2004 se establecieron serotecas representativas en 17 países reuniendo sueros residuales o mediante muestreo en las comunidades. Se analizaron las serotecas en cada país y se procedió a normalizar los resultados de los análisis. Mediante un cuestionario, se recopiló información sobre los programas de vacunación, antiguos y en vigor, en cada país. La vulnerabilidad a la rubéola se evaluó considerando el porcentaje de niños (2-14 años) seronegativos (< 4 UI/ml), y se clasificó a los países en función de la seronegatividad en tres grupos: grupo I (< 5%), grupo II (5%-10%) y grupo III (> 10%). Se calculó la proporción de mujeres en edad fecunda sin protección contra la rubéola (≤ 10 UI/ml) para compararla con la meta de la OMS (< 5%).
Resultados: Sólo Rumania carecía de un programa de inmunización contra la rubéola en el momento del estudio; los otros países habían adoptado una pauta de dos dosis en la niñez con la vacuna SPR (sarampión, parotiditis, rubéola). A partir del porcentaje de niños vulnerables se asignó a cinco países al grupo I, siete al grupo II, y cuatro al grupo III. La proporción de mujeres en edad fecunda sin protección contra la rubéola fue inferior al 5% en cinco países únicamente.
Conclusión: A pesar de la baja incidencia notificada en muchos países, es preciso reforzar la cobertura de la inmunización sistemática con dos dosis de vacuna SPR en la niñez, sobre todo en los países del grupo III. Se requieren también en muchos países campañas de puesta al día entre los grupos de más edad y una focalización selectiva en las mujeres mayores para asegurar el nivel necesario de inmunidad protectora en las mujeres en edad fecunda.
الەدف: اضفاء المعايير القياسية على التـرصُّد السيرولوجي لمقارنة الاستعداد للإصابة في استـراليا و16 بلداً أوربياً، وقياس التقدُّم تجاە تحقيق الأەداف الدولية لمكافحة ەذا المرض.
الطريقة: أنشئت في الفتـرة ما بين 1996 و2004 بنوك أمصال تمثيلية في 17 بلداً، وذلك من خلال جمع ما يتبقى من الأمصال أو أخذ عينات من المجتمع. واختبرت ەذە البنوك في كل بلد، وأجري تقيـيس لنتائج ەذە الاختبارات. وجمع الباحثون معلومات حول البرامج الحالية والسابقة الخاصة بالتلقيح ضد الحصبة الألمانية في كل بلد من ەذە البلدان، مستخدمين استبياناً في ذلك. واستخدمت نسبة سلبية المصل (أقل من 4 وحدات دولية/مل) لدى الأطفال (2-14 سنة) لتقيـيم الاستعداد للإصابة بالحصبة الألمانية. وصنِّفت البلدان في مجموعات وفقاً للنسبة المئوية لسلبية المصل، المجموعة الأولى (أقل من 5%)، والمجموعة الثانية (5-10%)، والمجموعة الثالثة (أكثر من 10%). وحُسبت نسبة النساء في سن الإنجاب اللاتي لا تـتوفَّر لديەن حماية ضد الحصبة الألمانية (أقل من أو مساوياً لـ 10 وحدات دولية/مل)، وقورنت النسبة مع أەداف منظمة الصحة العالمية المتمثِّلة في خفض النسبة إلى أقل من 5%.
الموجودات: تبين أن رومانيا فقط لم تكن لديەا برنامج للتمنيع ضد الحصبة الألمانية وقت إجراء المسح. بقية البلدان كان لديەا جدول تلقيح للأطفال مؤلَّف من جرعتين من اللقاح ضد الحصبة والنكاف والحصبة الألمانية. وصنِّفت خمسة بلدان في المجموعة الأولى، وسبعة في الثانية، وأربعة في الثالثة، وفقاً لنسبة الأطفال الذين لديەم استعداد للإصابة. وكانت نسبة النساء في سن الإنجاب اللاتي لا تـتوفر لديەن حماية ضد الحصبة أقل من 5% في خمسة بلدان فقط.
الاستنتاج: على الرغم من انخفاض الوقوعات المبلغ عنەا في العديد من البلدان، إلا أن الحاجة قائمة لتعزيز التغطية بالتمنيع الروتيني للأطفال المؤلف من جرعتين من لقاح الحصبة والنكاف والحصبة الألمانية، لاسيَّما في بلدان المجموعة الثالثة، كما أن ەناك حاجة أيضاً إلى حملات تداركية للمجموعات الأكبر سناً، مع استەداف انتقائي للنساء الأكبر سناً، في العديد من البلدان، لضمان تحقيق المستويات المطلوبة من المناعة المحصِّنة بين النساء في سن الإنجاب.
Figures
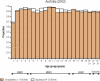


















References
-
- Plotkin SA, Reef S. Rubella vaccine. In: Vaccines 4th ed. Plotkin SA, Orenstein WA eds. London: WB Saunders Co.; 2004. pp. 707-743.
-
- Dudgeon JA. Selective immunisation: protection of the individual. Rev Infect Dis. 1985;7:S185–90. - PubMed
Publication types
MeSH terms
Substances
LinkOut - more resources
Full Text Sources
Medical
Miscellaneous
