Neoadjuvant chemoradiation therapy with gemcitabine/cisplatin and surgery versus immediate surgery in resectable pancreatic cancer: results of the first prospective randomized phase II trial
- PMID: 25252602
- PMCID: PMC4289008
- DOI: 10.1007/s00066-014-0737-7
Neoadjuvant chemoradiation therapy with gemcitabine/cisplatin and surgery versus immediate surgery in resectable pancreatic cancer: results of the first prospective randomized phase II trial
Abstract
Background: In nonrandomized trials, neoadjuvant treatment was reported to prolong survival in patients with pancreatic cancer. As neoadjuvant chemoradiation is established for the treatment of rectal cancer we examined the value of neoadjuvant chemoradiotherapy in pancreatic cancer in a randomized phase II trial. Radiological staging defining resectability was basic information prior to randomization in contrast to adjuvant therapy trials resting on pathological staging.
Patients and methods: Patients with resectable adenocarcinoma of the pancreatic head were randomized to primary surgery (Arm A) or neoadjuvant chemoradiotherapy followed by surgery (Arm B), which was followed by adjuvant chemotherapy in both arms. A total of 254 patients were required to detect a 4.33-month improvement in median overall survival (mOS).
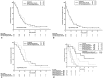
Results: The trial was stopped after 73 patients; 66 patients were eligible for analysis. Twenty nine of 33 allocated patients received chemoradiotherapy. Radiotherapy was completed in all patients. Chemotherapy was changed in 3 patients due to toxicity. Tumor resection was performed in 23 vs. 19 patients (A vs. B). The R0 resection rate was 48% (A) and 52% (B, P = 0.81) and (y)pN0 was 30% (A) vs. 39% (B, P = 0.44), respectively. Postoperative complications were comparable in both groups. mOS was 14.4 vs. 17.4 months (A vs. B; intention-to-treat analysis; P = 0.96). After tumor resection, mOS was 18.9 vs. 25.0 months (A vs. B; P = 0.79).
Conclusion: This worldwide first randomized trial for neoadjuvant chemoradiotherapy in pancreatic cancer showed that neoadjuvant chemoradiation is safe with respect to toxicity, perioperative morbidity, and mortality. Nevertheless, the trial was terminated early due to slow recruiting and the results were not significant. ISRCTN78805636; NCT00335543.
Hintergrund: Mehrere nichtrandomisierte Studien zeigten, dass eine neoadjuvante Therapie das Überleben bei Patienten mit Pankreaskarzinom verlängert. Beim lokal fortgeschrittenen Rektumkarzinom gehört die neoadjuvante Radiochemotherapie bereits zum Therapiestandard. Analog wurde der Stellenwert einer Radiochemotherapie beim Pankreaskarzinom in einer randomisierten Phase-II-Studie untersucht. Das prätherapeutische radiologische Staging war Grundlage dieser Studie im Gegensatz zu adjuvanten Therapiestudien, die auf pathohistologischem Staging basieren.
Patienten und Methoden: Patienten mit resektablem Pankreaskopfkarzinom wurden randomisiert in primäre Operation (Arm A) versus neoadjuvante Radiochemotherapie gefolgt von einer Operation (Arm B). Beide Gruppen erhielten eine adjuvante Chemotherapie. Es waren 254 Patienten erforderlich, um eine Verbesserung des medianen Gesamtüberlebens von 4,33 Monaten zu erfassen.
Ergebnisse: Die Studie wurde wegen zögerlicher Rekrutierung nach Einschluss von 73 Patienten beendet. Insgesamt konnten 66 Patienten ausgewertet werden. Die ihnen zugeordnete Radiochemotherapie erhielten 29 von 33 Patienten. Alle Patienten bekamen die vollständige Bestrahlungstherapie. Wegen der Toxizität wurde bei 3 Patienten die Chemotherapie reduziert. Eine Pankreastumorresektion erhielten 23 vs. 19 Patienten (A vs. B). Die R0-Resektionsrate betrug 48 % (A) und 52 % (B, P = 0,81). Bei 30 % (A) versus 39 % (B, P = 0,44) der resezierten Patienten waren keine Lymphknotenmetastasen vorhanden. Die postoperativen Komplikationen waren in beiden Gruppen vergleichbar. Das mediane Gesamtüberleben betrug 14,4 vs. 17,4 Monate (A vs. B; „Intention-to-treat“-Analyse; P = 0,96). Nach Pankreastumorresektion stieg das Gesamtüberleben auf 18,9 vs. 25,0 Monate (A vs. B; P = 0,79).
Schlussfolgerung: Diese weltweit erste randomisierte Studie zur neoadjuvanten Radiochemotherapie beim Pankreaskopfkarzinom war in Bezug auf Toxizität sowie perioperative Morbidität und Mortalität gut durchführbar. Die Ergebnisse sind jedoch nicht signifikant, da diese randomisierte Studie vorzeitig wegen mangelnder Rekrutierung beendet werden musste. ISRCTN78805636; NCT00335543.
Figures

References
-
- Glimelius B, Pahlman L, Cervantes A. Rectal cancer: ESMO Clinical Practice guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2010;21(5):8. - PubMed
Publication types
MeSH terms
Substances
Associated data
LinkOut - more resources
Full Text Sources
Other Literature Sources
Medical

