Evaluation of clinical trials by Ethics Committees in Germany--results and a comparison of two surveys performed among members of the German Association of Research-Based Pharmaceutical Companies (vfa)
- PMID: 25698912
- PMCID: PMC4311050
- DOI: 10.3205/000206
Evaluation of clinical trials by Ethics Committees in Germany--results and a comparison of two surveys performed among members of the German Association of Research-Based Pharmaceutical Companies (vfa)
Abstract
Objective: The objective of this project was to evaluate the quality and quantity of initial applications for a clinical trial according to § 7 of the German Good Clinical Practice (GCP) ordinance (German: GCP-Verordnung, GCP-V), the quality of evaluations of those applications by Ethics Committees (ECs)/Investigational Review Boards (IRBs) in Germany as well as the pattern of EC objections in their reasoned opinions (vote). In order to identify a change over time, the results of the present survey were also compared with a survey performed in 2008.
Methods: Based on reasoned opinions issued by the respective EC in charge of the coordinating principle investigator (coordinating EC) in 2011, a written survey among members of the German Association of Research-Based Pharmaceutical Companies (vfa) was conducted in 2012. The answers to the questionnaire were analyzed descriptively. Since the data set collected in 2011 was structurally identical with the data set gained in 2007 both surveys were compared.
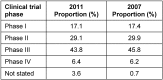
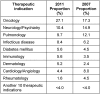
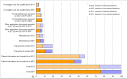
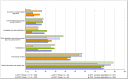
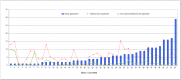
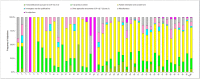
Results: Of the 24 companies represented on the vfa Clinical Research/Quality Assurance Subcommittee, 75% (18) took part in the survey. Survey evaluation was based on a total of 251 applications of these 18 companies submitted to 43 ECs. These account for about 21% of 1,214 applications for authorization of commercial and non-commercial phase I-IV clinical trials submitted to the regulatory authorities (BfArM and PEI) in 2011. In comparison to 2007, a lower amount of applications (n=251 in 2011 vs. n=288 in 2007) was submitted to a slightly higher number of ECs (43 in 2011 vs. 40 in 2007). The amount of objections increased by 21% from 1,299 (2007) to 1,574 (2011) resulting in an average of 4.5 (2007) vs. 6.3 (2011) objections per application. Overall, the analysis of both formal and content related objections revealed almost the same pattern as in the previous survey. In total, the most frequent objections applied to the patient information and consent form followed in descending order by trial protocol content, miscellaneous, other application documents pursuant to § 7 (2) and (3) GCP-V, formal deficiencies pursuant to § 8 (1) GCP-V, and investigator and site qualifications. A trend towards a slightly increased rate of objections concerning patient information and consent form (+4%) and a minimal decrease in objections concerning investigator and site qualifications (-2%) was observed. As in 2007, about 1 in 6 applications was still incomplete with formal objections. Whilst the proportion of study applications with objections related to the patient information and consent form (+7.2%), the trial protocol content (+11.6%), and documents according to § 7 (2) and (3) GCP-V (+11.8%) increased in 2011 compared to 2007, the amount of study applications with objections related to the investigator and site qualifications decreased by 6.3%.
Conclusions: The majority of findings with respect to quantity, quality and main focus of objections reported in the first survey in 2008 were also found in 2012, indicating a shared understanding of applicable measures and criteria by sponsors and ECs on how to ensure patient rights and well-being, data integrity, and high quality documentation in clinical trials.
Ziel: Das Ziel dieses Projektes war es, die Qualität und Quantität der Erstantragstellung auf zustimmende Bewertung einer klinischen Prüfung gemäß § 7 der deutschen GCP-Verordnung (GCP-V), die Qualität des Bewertungsverfahrens bei den Ethik-Kommissionen (EKs) in Deutschland sowie das Muster der Einwände seitens der EKs in ihren mit Gründen versehenen Bewertungen (Bescheide) zu evaluieren. Um etwaige Veränderungen über die Zeit zu identifizieren, wurden außerdem die Ergebnisse dieser Umfrage, mit den Ergebnissen einer in 2008 durchgeführten Umfrage verglichen.Methoden: Auf der Grundlage von Bescheiden der für den Leiter der klinischen Prüfung jeweils zuständigen (federführenden) EK in 2011, wurde eine schriftliche Umfrage bei Mitgliedsunternehmen des Verbandes Forschender Arzneimittelhersteller e.V. (vfa) in 2012 durchgeführt. Die erhaltenen Antworten zu dem Fragebogen wurden deskriptiv ausgewertet. Da der in 2011 erhaltene Datensatz mit dem Datensatz in 2007 strukturell identisch war, wurden beide Umfragen miteinander verglichen.Ergebnisse: Von den 24 Unternehmen, die im vfa-Unterausschuss Klinische Forschung/Qualitätssicherung vertreten sind, nahmen 75% (18) an der Umfrage teil. Der Auswertung dieser Umfrage liegen insgesamt 251 Antragsverfahren dieser 18 Unternehmen bei 43 EKs zugrunde. Diese stellen rund 21% der 1.214 bei den Bundesoberbehörden (BfArM und PEI) 2011 gestellten Anträge auf Genehmigung kommerzieller und nicht-kommerzieller klinischer Prüfungen der Phasen I–IV dar.Im Vergleich zu 2007 wurden 2011 eine geringere Zahl von Anträgen (n=251 in 2011 vs. n=288 in 2007) bei einer geringfügig größeren Zahl an EKs (43 in 2011 vs. 40 in 2007) gestellt. Die Anzahl der Einwände stieg um 21% von 1.299 (2007) auf 1.574 (2011) und damit im Durchschnitt von 4,5 (2007) auf 6,3 (2011) Einwände pro Antrag. Insgesamt gesehen zeigt die Analyse der formalen und inhaltlichen Einwände ein Muster auf, das der vorangegangenen Umfrage sehr ähnlich ist. Die häufigsten Einwände betreffen die Patienteninformation und Einwilligungserklärung, in absteigender Reihenfolge gefolgt von Einwänden bezüglich Prüfplaninhalten, nicht-kategorisierende Einwände („Andere“), Einwände zu „Sonstigen Antragsunterlagen“ nach § 7 (2) und (3) GCP-V, Formmängel nach § 8 (1) GCP-V sowie Einwände, die sich auf Unterlagen zur Prüfer- und Prüfstellenqualifikation beziehen. Tendenziell zu beobachten war eine leicht erhöhte Rate von Einwänden bezüglich der Patienteninformation und Einwilligungserklärung (+4%) sowie eine geringfügige Abnahme von Einwänden, die sich auf Unterlagen zur Prüfer- und Prüfstellenqualifikation bezogen (–2%).Wie in 2007 ist etwa jeder sechste Antrag unvollständig und weist formale Einwände zu den Antragsunterlagen auf. Während der Anteil der Studienanträge mit Einwänden bezüglich der Patienteninformation und Einwilligungserklärung (+7,2%), den Prüfplaninhalten (+11,6%) und „Sonstigen Antragsunterlagen“ nach § 7 (2) und (3) GCP-V (+11,8%) in 2011 im Vergleich zu 2007 zunahm, nahm der Anteil der Studienanträge mit Einwänden, die Unterlagen zur Prüfer- und Prüfstellenqualifikation betrafen, um 6,3% ab.Schlussfolgerungen: Die Ergebnisse der ersten Umfrage in 2008 im Hinblick auf die Quantität, die Qualität und die Schwerpunkte der Einwände seitens der EKs, finden sich überwiegend auch in der Umfrage 2012. Dies zeigt ein übereinstimmendes Verständnis von Auftraggebern (Sponsoren) und EKs hinsichtlich der anzuwendenden Maßnahmen und Kriterien zur Sicherstellung der Rechte und des Wohlergehens der Patienten, der Datenintegrität und einer qualitativ hochwertigen Dokumentation in klinischen Prüfungen.
Keywords: Ethics Committees; application procedure; clinical trials; formal and content-related objections.
Figures

References
-
- Russ H, Busta S, Riedel A, Zoellner G, Jost B. Evaluation of clinical trials by Ethics Committees in Germany Experience of applicants with the review of requests for opinion of the Ethics Committees – results of a survey among members of the German Association of Research-Based Pharmaceutical Companies (VFA) GMS Ger Med Sci. 2009;7:Doc07. doi: 10.3205/000066. Available from: http://dx.doi.org/10.3205/000066. - DOI - DOI - PMC - PubMed
-
- Verordnung über die Anwendung der Guten Klinischen Praxis bei der Durchführung von klinischen Prüfungen mit Arzneimitteln zur Anwendung am Menschen (GCP-Verordnung – GCP-V) vom 9. August 2004, zuletzt geändert am 19. Oktober 2012. [Ordinance on the implementation of Good Clinical Practice in the conduct of clinical trials on medicinal products for use in humans (GCP Ordinance – GCP-V) of 9 August 2004, latest version as of 19 October 2012]. Bundesgesetzblatt. 2004;Teil I(42):2081. (Ger). Available from: http://www.gesetze-im-internet.de/gcp-v/
-
- Bundesinstitut für Arzneimittel und Medizinprodukte [Federal Institute for Drugs and Medical Devices] Statistik: Anträge auf Genehmigung einer Klinischen Prüfung. Available from: http://www.bfarm.de/DE/Arzneimittel/zul/klinPr/klin_prf_genehm/Statistik....
-
- Paul-Ehrlich-Institut. Bearbeitungsstatistiken für Anträge auf klinische Prüfung am Paul Ehrlich-Institut [Statistics on the request for clinical trial authorisations] Langen: PEI; [created: 2006 July 18; updated: 2014 July 28]. Available from: http://www.pei.de/DE/infos/pu/genehmigung-klinische-pruefung/bearbeitung....
-
- Bundesinstitut für Arzneimittel und Medizinprodukte [Federal Institute for Drugs and Medical Devices] Genehmigungsverfahren Statistik. Bonn: BfArM; [updated: 2008 Feb 26; cited 2009 Jul 07].
Publication types
MeSH terms
LinkOut - more resources
Full Text Sources
Medical
Research Materials

