Does age matter? The impact of rodent age on study outcomes
- PMID: 27307423
- PMCID: PMC5367550
- DOI: 10.1177/0023677216653984
Does age matter? The impact of rodent age on study outcomes
Abstract
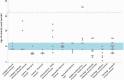
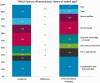
Rodent models produce data which underpin biomedical research and non-clinical drug trials, but translation from rodents into successful clinical outcomes is often lacking. There is a growing body of evidence showing that improving experimental design is key to improving the predictive nature of rodent studies and reducing the number of animals used in research. Age, one important factor in experimental design, is often poorly reported and can be overlooked. The authors conducted a survey to assess the age used for a range of models, and the reasoning for age choice. From 297 respondents providing 611 responses, researchers reported using rodents most often in the 6-20 week age range regardless of the biology being studied. The age referred to as 'adult' by respondents varied between six and 20 weeks. Practical reasons for the choice of rodent age were frequently given, with increased cost associated with using older animals and maintenance of historical data comparability being two important limiting factors. These results highlight that choice of age is inconsistent across the research community and often not based on the development or cellular ageing of the system being studied. This could potentially result in decreased scientific validity and increased experimental variability. In some cases the use of older animals may be beneficial. Increased scientific rigour in the choice of the age of rodent may increase the translation of rodent models to humans.
Les modèles murins produisent des données qui sous-tendent la recherche biomédicale ainsi que les essais non-cliniques de médicaments, mais il est rare que les données issues des rongeurs se transforment en résultats cliniques réussis. Il existe un nombre croissant de preuves montrant que l’amélioration de la conception expérimentale est essentielle à l’amélioration de la nature prédictive des études menées sur des rongeurs, ainsi qu’à la réduction du nombre d’animaux utilisés en recherche. L’âge, un facteur important dans la conception expérimentale, est souvent mal pris en compte dans les rapports et peut être négligé. Les auteurs ont mené une enquête pour évaluer l’âge utilisé dans une gamme de modèles, et le raisonnement motivant le choix de l’âge. D’après les 297 répondants fournissant 611 réponses, les chercheurs ont constaté que les rongeurs utilisés avaient le plus souvent de 6 à 20 semaines d’âge, indépendamment de la biologie faisant l’objet de l’étude. L’âge que les répondants estimaient « adulte » variait entre 6 et 20 semaines. Des raisons pratiques justifiant le choix de l’âge des rongeurs ont été fréquemment avancées, l’augmentation des coûts liés à l’utilisation d’animaux plus âgés et le maintien de la comparabilité des données historiques étant deux importants facteurs limitatifs. Ces résultats mettent en lumière que le choix de l’âge n’est pas uniforme au sein de la communauté scientifique et qu’il est rarement fondé sur le développement ou le vieillissement cellulaire du système étudié. Cela pourrait entraîner une diminution de la validité scientifique et une augmentation de la variabilité expérimentale. Dans certains cas, l’utilisation d’animaux plus âgés peut s’avérer bénéfique. La rigueur scientifique accrue dans le choix de l’âge des rongeurs peut augmenter l’application de modèles de rongeurs à l’homme.
Nagermodelle liefern Daten zur Untermauerung biomedizinischer Forschung und nicht-klinischer Arzneimittelprüfungen, doch an einer Übertragung von mit Nagern erzielten Resultaten in erfolgreiche klinische Ergebnisse mangelt es häufig. Es gibt zunehmend Belege dafür, dass die Verbesserung der Versuchsgestaltung der Schlüssel für bessere vorausschauende Aussagen von Nagerstudien und für eine Senkung der Zahl von Versuchstieren ist. Das Alter, ein wichtiger Faktor für die Versuchsgestaltung, wird oft ungenügend vermerkt und beachtet. Die Autoren führten eine Befragung zur Bewertung des Alters von bei verschiedenen Modellen verwendeten Tieren und die Gründe für die jeweilige Altersentscheidung durch. Dabei gaben 297 Befragte 611 Antworten. Die Forscher berichteten, dass sie meist Nager im Altersbereich von 6 bis 20 Wochen verwendeten, unabhängig vom zu untersuchenden biologischen Gegenstand. Das von Befragten als ,,adult“ bezeichnete Alter variierte zwischen sechs und 20 Wochen. Für die Wahl des Nageralters wurden häufig praktische Gründe angeführt, wobei erhöhte Kosten bei der Nutzung älterer Tiere und die Vergleichbarkeit historischer Daten als zwei hemmende Faktoren genannt wurden. Diese Ergebnisse zeigen, dass Forscher keine einheitlichen Kriterien bei der Wahl des Alters anlegen und dass ihre Wahl häufig nicht auf der Entwicklung oder Zellalterung des untersuchten Systems basiert. Daraus könnte potenziell eine reduzierte wissenschaftliche Gültigkeit und erhöhte experimentelle Variabilität resultieren. In manchen Fällen kann u. U. die Verwendung älterer Tiere von Vorteil sein. Erhöhte wissenschaftliche Stringenz bei der Wahl des Alters von Nagern kann u. U. der Übertragung von Nagermodellen auf Menschen förderlich sein.
Los modelos de ratones producen datos que respaldan la investigación biomédica y pruebas de fármacos no clínicas, pero muchas veces falta la conversión de roedores a unos resultados clínicos fructíferos. Existe cada vez más evidencia de que la mejora del diseño experimental es clave para mejorar la naturaleza predictiva de los estudios con roedores y para reducir el número de animales utilizado en estudios de investigación. La edad, un factor importante en el diseño experimental, no se registra adecuadamente con frecuencia y puede pasarse por alto. Los autores llevaron a cabo un estudio para evaluar la edad utilizada para una serie de modelos y el razonamiento detrás de la elección de distintas edades. De 297 participantes que aportaron 611 respuestas, los investigadores registraron un uso frecuente de roedores de entre 6 y 20 semanas de edad, independientemente de su estudio biológico. La edad considerada como "adulta" por parte de los participantes variaba de entre 6 y 20 semanas. Con frecuencia se registró que la elección de las edades de los roedores se debe a motivos prácticos, con un aumento del coste asociado con el uso de animales mayores y el mantenimiento de la comparabilidad de datos históricos siendo dos factores decisivos. Estos resultados destacaron que la elección de edad es inconsistente en la comunidad de investigadores y a menudo no se basa en el desarrollo o el envejecimiento celular del sistema estudiado. Esto potencialmente podría provocar una reducción de la validez científica y un aumento de la variabilidad experimental. En algunos casos, el uso de animales mayores podría ser beneficioso. Un mayor rigor científico en la elección de la edad de los roedores podría aumentar la conversión de modelos de roedores a humanos.
Keywords: age; development; experimental design; rodent; senescence.
Figures

References
-
- Festing MF, Altman DG. Guidelines for the design and statistical analysis of experiments using laboratory animals. ILAR J 2002; 43: 244–258. - PubMed
-
- Talevi A, Bellera CL, Di Ianni M, Gantner M, Bruno-Blanch LE, Castro EA. CNS drug development – lost in translation? Mini Rev Med Chem 2012; 12: 959–970. - PubMed
MeSH terms
Grants and funding
LinkOut - more resources
Full Text Sources
Other Literature Sources
Medical

