LPS-matured CD11c+ bone marrow-derived dendritic cells can initiate autoimmune pathology with minimal injection site inflammation
- PMID: 27488372
- PMCID: PMC5431364
- DOI: 10.1177/0023677216663584
LPS-matured CD11c+ bone marrow-derived dendritic cells can initiate autoimmune pathology with minimal injection site inflammation
Abstract
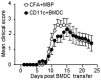
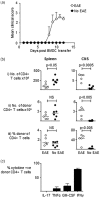
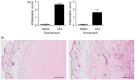
The pathogenesis of human autoimmune disorders is incompletely understood. This has led to the development of numerous murine models in which the pathogenesis of autoimmunity can be probed and the efficacy of novel therapies can be tested. One of the most widely-used murine models of autoimmunity is experimental autoimmune encephalomyelitis (EAE). To induce autoimmune pathology, mice are often immunized with an autoantigen alongside an adjuvant, typically complete Freund's adjuvant (CFA). Unfortunately, CFA causes significant inflammation at the site of administration. Despite the well-recognized complication of injection site inflammation, CFA with autoantigen immunization is widely used to induce central nervous system autoimmunity. We performed a literature review which allowed us to estimate that over 10,000 mice were immunized with CFA in published EAE studies in 2013. In this study, we demonstrated that subcutaneously administered myelin basic protein (MBP)-pulsed CD11c+ bone marrow-derived dendritic cells (BMDC) were as effective at inducing EAE as subcutaneously administered MBP plus CFA. Importantly, we also discovered that the CD11c+ BMDC caused significantly less injection site inflammation than MBP plus CFA immunization. This study demonstrated that the use of CD11c+ BMDC can enable the development of autopathogenic T-cells to be studied in vivo without the unwanted side-effects of long-lasting injection site inflammation. This model represents a significant refinement to existing EAE models and may lead to the improvement of the welfare of experimental mice used to study the development of autoimmunity in vivo.
La pathogénèse des troubles humains auto-immuns n’est pas entièrement comprise. Cela a conduit au développement de nombreux modèles murins dans lesquels la pathogénèse de l’auto-immunité peut être prouvée et l’efficacité de nouvelles thérapies peut être testée. L’encéphalomyélite auto-immune expérimentale (EAE) est un des modèles murins d'auto-immunité les plus largement utilisés. Pour induire la pathologie auto-immune, des souris sont souvent immunisées avec un auto-antigène associé à un adjuvant, typiquement l’adjuvant complet de Freund (ACF). Malheureusement l’ACF provoque une inflammation importante au niveau du site d’injection. En dépit de la complication déjà connue de l’inflammation du site d’injection, l’ACF associé à l’immunisation auto-antigène est largement utilisée pour induire l’auto-immunité du système nerveux central. Nous avons réalisé une synthèse de la littérature scientifique qui nous a permis d’évaluer que plus de 10 000 souris avaient été immunisées avec l’ACF dans des études publiées sur l’EAE en 2013. Dans cette étude, nous avons démontré que l’injection de cellules dentritiques dérivées de la moelle osseuse (BMDC) CD11cþ pulsées avec de la protéine basique de la myéline (MBP) par voie sous-cutanée était aussi efficace pour induire l’EAE que l’association MBP plus ACF administrée par voie sous cutanée. Autre fait important, nous avons aussi découvert que les BMDDC CD11cþ provoquaient une inflammation moins importante du site d’injection que l’immunisation MBP plu ACF. Cette étude a démontré que l’utilisation de BMDC CD11cþ pouvait permettre d'étudier le développement auto-pathogène des cellules-T in vivo sans les effets secondaires indésirables de l’inflammation à long terme au site d’injection. Ce modèle représente une amélioration importante par rapport aux modèles EAE et peut conduire à une amélioration du bien-être des souris de laboratoire utilisées pour observer le développement de l’auto-immunité in vivo.
Die Pathogenese von Autoimmunerkrankungen des Menschen ist bisher nicht vollständig geklärt. Dies führte zur Entwicklung zahlreicher Maus-Modelle, mit denen die Pathogenese von Autoimmunität untersucht und die Wirksamkeit neuartiger Therapien getestet werden kann. Eines der am meisten verwendeten Autoimmunitäts-Maus-Modelle ist experimentelle Autoimmun-Encephalomyelitis (EAE). Zur Induzierung von Autoimmun-Pathologie werden Mäuse häufig mit einem Autoantigen zusammen mit einem Adjuvans, zumeist dem kompletten Freund-Adjuvans (KFA), immunisiert. Leider verursacht KFA signifikante Entzündung an der Stelle der Verabreichung. Trotz dieser weithin bekannten Komplikation der Injektionsstellenentzündung wird KFA mit Auotantigen-Immunisierung sehr oft zur Induzierung von Autoimmunität des zentralen Nervensystems verwendet. Von uns durchgeführte Literaturstudien ermöglichten uns einzuschätzen, dass veröffentlichten EAE-Studien zufolge 2013 über 10.000 Mäuse mit KFA immunisiert wurden. In der vorliegenden Studie wiesen wir nach, dass subkutan verabreichte Myelin-Basische Protein (MBP)-gepulste aus Knochenmark abgeleitete CD11cþ dendritische Zellen (BMDC) ebenso wirksam bei der Induzierung von EAE sind wie subkutan zusammen mit KFA verabreichtes MBP. Es ist wichtig zu betonen, dass wir feststellten, dass die CD11cþ BMDC signifikant weniger Injektionsstellenentzündung verursachten als Immunisierung mit MBP und KFA. Diese Studie zeigte, dass die Verwendung von CD11cþ BMDC die Entwicklung von in-vivo zu untersuchenden autopathogenen T-Zellen ermöglichen kann ohne die unerwünschten Nebenwirkungen langanhaltender Injektionsstellenentzündung. Dieses Modell stellt eine entscheidende Verbesserung existierender EAE-Modelle dar und kann möglicherweise zu erhöhtem Wohlbefinden von Versuchsmäusen beitragen, die zu In-Vivo-Studien der Entwicklung von Autoimmunität dienen.
La patogénesis de los trastornos autoinmunes humanos no se conoce por completo. Esto ha llevado al desarrollo de numerosos modelos murinos en los que la patogénesis de la autoinmunidad puede explorarse y en los que la eficacia de terapias nuevas pueden probarse. Uno de los modelos murinos más utilizados de autoinmunidad es la encefalomielitis autoinmune experimental (EAE). Para inducir una patología autoinmune, normalmente se inmunizan a los ratones con un autoantígeno junto con un adyuvante, normalmente el adyuvante completo de Freund (CFA). Desafortunadamente, CFA causa una inflamación significativa en el lugar de la administración. A pesar de la bien conocida complicación de la inflamación del lugar de la inyección, la inmunización con CFA y autoantígeno es ampliamente utilizada para inducir autoinmunidad del sistema nervioso central. Llevamos a cabo una revisión de la literatura que nos permitió estimar que más de 10.000 ratones fueron inmunizados con CFA en estudios sobre EAE publicados en 2013. En este estudio, demostramos que la administración subcutánea de células dendríticas derivadas de la médula ósea CD11cþ con proteina básica de mielina [(MBP)-pulsed] fue tan eficaz para inducir EAE como la MBP administrada subcutáneamente más CFA. Asimismo, también descubrimos que CD11cþ BMDC causó una inflamación del lugar de la infección mucho menor que la inmunización con MBP más CFA. Este estudio demostró que el uso de CD11cþ BMDC puede permitir el desarrollo de células T autopatogénicas para ser estudiadas in vivo sin los efectos secundarios no deseados de la inflamación de larga duración del lugar de la inyección. Este modelo representa un refinamiento significativo de los modelos de EAE existentes y podría suponer una mejora del bienestar de los ratones de experimentación utilizados en el estudio del desarrollo de la autoinmunidad in vivo.
Keywords: autoimmune; bone marrow dendritic cells; complete Freund's adjuvant; experimental autoimmune encephalomyelitis; mice; refinement.
Figures
References
-
- Zhang W, Anis AH. The economic burden of rheumatoid arthritis: beyond health care costs. Clin Rheumatol 2011; 30(Suppl 1): S25–S32. - PubMed
-
- Olesen J, Gustavsson A, Svensson M, Wittchen HU, Jonsson B. The economic cost of brain disorders in Europe. Eur J Neurol 2012; 19: 155–162. - PubMed
-
- Wekerle H, Flugel A, Fugger L, Schett G, Serreze D. Autoimmunity's next top models. Nat Med 2012; 18: 66–70. - PubMed
-
- Bartholomaus I, Kawakami N, Odoardi F, et al. Effector T cell interactions with meningeal vascular structures in nascent autoimmune CNS lesions. Nature 2009; 462: 94–98. - PubMed
MeSH terms
Substances
Grants and funding
LinkOut - more resources
Full Text Sources
Other Literature Sources
Research Materials
Miscellaneous

