Disorders of spermatogenesis: Perspectives for novel genetic diagnostics after 20 years of unchanged routine
- PMID: 29527098
- PMCID: PMC5838132
- DOI: 10.1007/s11825-018-0181-7
Disorders of spermatogenesis: Perspectives for novel genetic diagnostics after 20 years of unchanged routine
Abstract
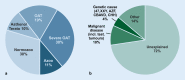
Infertility is a common condition estimated to affect 10-15% of couples. The clinical causes are attributed in equal parts to the male and female partners. Diagnosing male infertility mostly relies on semen (and hormone) analysis, which results in classification into the two major phenotypes of oligo- and azoospermia. The clinical routine analyses have not changed over the last 20 years and comprise screening for chromosomal aberrations and Y‑chromosomal azoospermia factor deletions. These tests establish a causal genetic diagnosis in about 4% of unselected men in infertile couples and 20% of azoospermic men. Gene sequencing is currently only performed in very rare cases of hypogonadotropic hypogonadism and the CFTR gene is routinely analysed in men with obstructive azoospermia. Still, a large number of genes have been proposed to be associated with male infertility by, for example, knock-out mouse models. In particular, those that are exclusively expressed in the testes are potential candidates for further analyses. However, the genome-wide analyses (a few array-CGH, six GWAS, and some small exome sequencing studies) performed so far have not lead to improved clinical diagnostic testing. In 2017, we started to routinely analyse the three validated male infertility genes: NR5A1, DMRT1, and TEX11. Preliminary analyses demonstrated highly likely pathogenic mutations in these genes as a cause of azoospermia in 4 men, equalling 5% of the 80 patients analysed so far, and increasing the diagnostic yield in this group to 25%. Over the past few years, we have observed a steep increase in publications on novel candidate genes for male infertility, especially in men with azoospermia. In addition, concerted efforts to achieve progress in elucidating genetic causes of male infertility and to introduce novel testing strategies into clinical routine have been made recently. Thus, we are confident that major breakthroughs concerning the genetics of male infertility will be achieved in the near future and will translate into clinical routine to improve patient/couple care.
Etwa 10–15 % aller Paare erzielen auf natürlichem Weg keine Schwangerschaft und sind nach WHO-Definition als „sub-/infertil“ einzustufen. Klinische Ursachen werden bei diesen Paaren etwa zur Hälfte bei der Frau bzw. beim Mann nachgewiesen. Die klinischen Untersuchungen bei männlicher Infertilität beschränken sich derzeit auf Ejakulat- und Hormonuntersuchungen, die dann bei einer Vielzahl der Männer zur deskriptiven „Diagnose“ Oligozoo- oder Azoospermie führen, wodurch die Ursache der Infertilität des Paares erklärt werden kann. Der eigentliche Grund für die Spermatogenesestörung bleibt damit aber unklar. Die genetische Diagnostik bei infertilen Männern hat sich in den letzten 20 Jahren nicht weiter entwickelt und umfasst nach wie vor ausschließlich das Screening hinsichtlich Chromosomenstörungen und Y‑chromosomaler AZF-Deletionen. Diese beiden Untersuchungen finden die tatsächliche Ursache der Spermatogenesestörung bei etwa 4 % der unselektierten Männer und bei etwa 20 % der Männer mit Azoospermie. Gensequenzierungen werden hingegen bislang ausschließlich bei Patienten mit hypogonadotropem Hypogonadismus, einem umschriebenen, sehr seltenen Krankheitsbild, bzw. bei obstruktiver Azoospermie (CFTR-Analytik) durchgeführt. Andererseits wurden bereits viele Gene publiziert, in denen Mutationen potenziell zu einer Infertilität des Mannes führen können. Allerdings haben die bislang publizierten Daten und auch die genomweiten Analysen keine Erweiterung der klinischen Diagnostik erreicht. Seit Anfang 2017 haben wir drei Kandidatengene – NR5A1, DMRT1 und TEX11 – bei Männern mit Azoospermie sequenziert. Die vorläufigen Auswertungen ergaben vier wahrscheinlich pathogene Mutationen in diesen Genen. Dies entspricht 5 % der 80 bislang ausgewerteten Männer. Die kausalen Diagnosen steigen bei dieser Patientengruppe somit auf etwa 25 %. In den vergangenen Jahren wurden zunehmend weitere Kandidatengene publiziert. Gleichzeitig laufen mehrere große Studien bei infertilen Männern. Deswegen gehen wir davon aus, dass in naher Zukunft weitere klinisch relevante Erkenntnisse gewonnen werden, die dann auch Einzug in die Routinediagnostik finden und die Behandlung dieser Männer bzw. des Paares verbessern werden.
Keywords: Azoospermia; Male infertility; Oligozoospermia.
Conflict of interest statement
Compliance with ethical guidelinesF. Tüttelmann, C. Ruckert and A. Röpke declare that they have no competing interests. Approval was obtained from the Ethics Committee of the Medical Faculty in Münster. All participants gave informed written consent. The study was conducted in accordance with the Declaration of Helsinki in its most recent amended version.
Figures

References
-
- Behre HM, Bergmann M, Simoni M, Tüttelmann F. Endotext. South Dartmouth: MDText.com, Inc.; 2015. Primary Testicular Failure; p. 2000.
-
- Bergmann M, Kliesch S. Testicular biopsy and histology. In: Nieschlag E, Beere HM, Nieschlag S, editors. Andrology—Male Reproductive Health and Dysfunction. Heidelberg: Springer; 2010. pp. 155–167.
Publication types
LinkOut - more resources
Full Text Sources
Other Literature Sources
Miscellaneous
