[Development of animal experimental model for bacterial peritonitis]
- PMID: 31795629
- PMCID: PMC6987621
- DOI: 10.37201/req/064.2019
[Development of animal experimental model for bacterial peritonitis]
Abstract
Objective: The aim of the study was to develop a model of abdominal sepsis in the experimental animal.
Methods: Sprague-Dawley male rats of 5 weeks (N=39) were used. Initially, a pilot study (N = 9) was performed and distributed in 3 groups with 1cc inoculum of Escherichia coli ATCC 25922 intraperitoneally at concentrations of 10E8, 10E9 and 10E10 CFU. Subsequently, concentrations of 10E10 CFU are used in two groups of 3 rats with dilutions of 10 cc and 15 cc of distilled water respectively. Finally, a randomized trial of 24 rats was started in three treatment groups after intraperitoneal infection: Group I with physiological serum (N = 6), Group II with ceftriaxone (N = 9), Group III with ceftriaxone plus allicin (N = 9). Microbiological samples of blood and peritoneal fluid were made, as well as histopathological study of intraperitoneal organs (liver, diaphragm and peritoneum).
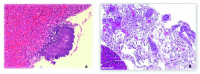
Results: Death of 100% of the rats infected with 10E10 E. coli UFC concentration with the dilution of 15 ml of distilled water and without antibiotic was oberved. The blood culture and peritoneal fluid culture was positive for the same strain in all of them. The formation of abscesses on the liver surface and polymorphonuclear infiltration in tissues were observed.
Conclusions: The lethal dose of E. coli is 10E10 CFU diluted in 15 cc distilled water by intraperitoneal injection.
Objetivo: Desarrollar un modelo de sepsis abdominal en animal de experimentación.
Material y métodos: Se utilizan ratas Sprague-Dawley®, machos de 5 semanas con pesos entre 270-280 g en el momento de la inoculación (N=39). Inicialmente se realiza un estudio piloto (N=9), distribuyéndolas en 3 grupos (3/3/3) con inóculo de 1cc de Escherichia coli ATCC 25922 intraperitoneal en concentraciones de 108, 109 y 1010 UFC. En un segundo estudio (N=6) con distribución en dos grupos (3/3) se utilizan 1cc una concentración de E. coli 1010 UFC que se diluyen en 10 y 15 ml de agua destilada para su inoculación. Por último se inicia un ensayo experimental con aleatorización de 24 ratas en tres grupos de tratamiento tras la infección intraperitoneal: Grupo I con suero fisiológico (N=6), Grupo II con antibiótico (ceftriaxona) (N=9), Grupo III con antibiótico más adyuvante (ceftriaxona más alicina) (N=9). Se realizan muestras microbiológicas de sangre y líquido peritoneal, así como estudio histopatológico de órganos intraperitoneales (hígado, diafragma y peritoneo).
Resultados: Se observa muerte en el 100% de las ratas infectadas con la concentración de E. coli 1010 UFC con la dilución de 15 ml de agua destilada y sin antibiótico. El hemocultivo y cultivo de líquido peritoneal es positivo a la misma cepa en todas ellas. Se observa la formación de abscesos en la superficie del hígado e infiltración por polimorfonucleares en los tejidos.
Conclusión: Se establece que la dosis letal de E. coli es 1010 UFC diluida en 15 ml agua destilada en inyección intraperitoneal.
Keywords: Escherichia coli; Sepsis; peritonitis; rats.
©The Author 2020. Published by Sociedad Española de Quimioterapia. This article is distributed under the terms of the Creative Commons Attribution-NonCommercial 4.0 International (CC BY-NC 4.0)(https://creativecommons.org/licenses/by-nc/4.0/).
Conflict of interest statement
Los autores declaran no tener ningún conflicto de intereses.
Figures

Similar articles
-
Development of an experimental model of induced bacterial peritonitis in cirrhotic rats with or without ascites.Am J Gastroenterol. 2007 Jun;102(6):1230-6. doi: 10.1111/j.1572-0241.2007.01182.x. Am J Gastroenterol. 2007. PMID: 17531011
-
The inoculum effect of Escherichia coli expressing mcr-1 or not on colistin activity in a murine model of peritonitis.Clin Microbiol Infect. 2019 Dec;25(12):1563.e5-1563.e8. doi: 10.1016/j.cmi.2019.08.021. Epub 2019 Sep 5. Clin Microbiol Infect. 2019. PMID: 31494253
-
[Inhibition of peritoneal bacterial adhesion using oligosaccharides. An experimental model of peritonitis in rats].Chirurgie. 1999 Apr;124(2):159-64. doi: 10.1016/s0001-4001(99)80059-2. Chirurgie. 1999. PMID: 10349753 French.
-
TLR4 inhibition impairs bacterial clearance in a therapeutic setting in murine abdominal sepsis.Inflamm Res. 2014 Nov;63(11):927-33. doi: 10.1007/s00011-014-0766-9. Epub 2014 Aug 15. Inflamm Res. 2014. PMID: 25118783
-
The use of local and systemic antibiotics in rat fecal peritonitis.J Surg Res. 1994 Sep;57(3):360-5. doi: 10.1006/jsre.1994.1155. J Surg Res. 1994. PMID: 8072283
Cited by
-
Black Garlic and Thiosulfinate-Enriched Extracts as Adjuvants to Ceftriaxone Treatment in a Rat Peritonitis Model of Sepsis.Biomedicines. 2022 Dec 1;10(12):3095. doi: 10.3390/biomedicines10123095. Biomedicines. 2022. PMID: 36551850 Free PMC article.
References
-
- van der Heijden KM, van der Heijden IM, Galvao FH, Lopes CG, Cos-ta SF, Abdala E, et al. . Intestinal translocation of clinical isolates of vancomycin-resistant Enterococcus faecalis and ESBL-producing Escherichia coli in a rat model of bacterial colonization and liver is-chemia/reperfusion injury. PLoS One 2014;9:e108453. doi:10.1371/journal.pone.0108453. - DOI - PMC - PubMed
MeSH terms
Substances
LinkOut - more resources
Full Text Sources
Medical

