[Novel platelet pharming using human induced pluripotent stem cells]
- PMID: 33012790
- PMCID: PMC7521593
- DOI: 10.1016/j.banm.2020.09.040
[Novel platelet pharming using human induced pluripotent stem cells]
Abstract
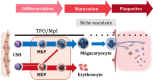
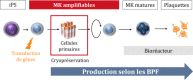
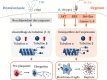
Ex vivo production of human platelets have been pursued as an alternative measure to resolve limitations in the supply and safety of current platelet transfusion products. To this end, induced pluripotent stem cells (iPSCs) are considered an ideal global source, since they are not only pluripotent and self-renewing, but also are available from basically any person, have relatively few ethical issues, and are easy to manipulate. From human iPSCs, megakaryocyte (MK) lines with robust proliferation capacity have been established by the introduction of specified sets of genes. These expandable MKs are also cryopreservable and thus would be suitable as master cells for good manufacturing practice (GMP) grade production of platelets, assuring availability on demand and safety against blood-borne infections. Meanwhile, developments in bioreactors that physically mimic the in vivo environment and discovery of substances that promote thrombopoiesis have yielded competent platelets with improved efficiency. The derivation of platelets from iPSCs could further resolve transfusion-related alloimmune complications through the manufacturing of autologous products and human leukocyte antigen (HLA)-compatible platelets by manipulation of HLAs and human platelet antigens (HPAs). Considering these key advances in the field, HLA-deleted platelets could become a universal product that is manufactured at industrial level to safely fulfill almost all demands. In this review, we overview the ex vivo production of iPSC-derived platelets towards clinical applications, a production that would revolutionize the blood transfusion system.
La production in vitro de plaquettes offre une opportunité de résoudre les problèmes liés aux limitations d’approvisionnement et à la sécurité des dons de produits dérivés du sang. Les cellules souches pluripotentes induites – ou iPSC – sont une source idéale pour la production de cellules à des fins de thérapies régénératives. Nous avons précédemment établi avec succès une lignée mégacaryocytaire immortalisée à partir d’iPSC. Celle-ci possède une capacité de prolifération fiable. Par ailleurs, il est possible de les cryoconserver. Elle est donc une source adaptée de cellules primaires pour la production de plaquettes suivant les Bonnes Pratiques de Fabrication (BPF). Dans le même temps, la capacité améliorée des bioréacteurs à reproduire certaines conditions physiologiques, telle que la turbulence, de pair avec la découverte de molécules favorisant la thrombopoïèse, a contribué à l’accomplissement de la production de plaquettes en quantité et qualité suffisantes pour répondre aux besoins cliniques. La production de plaquettes à partir de cellules iPS s’étend aussi aux patients en état de réfraction allo-immune, par la production de plaquettes autologues ou dont on a génétiquement manipulé l’expression des Antigènes des Leucocytes Humains (HLA) et des Antigènes Plaquettaires Humain (HPA). Considérant ces avancées fondamentales, les plaquettes iPSC avec expression des HLA modifiées se présentent comme un potentiel produit de transfusion universel. Dans cette revue, nous souhaitons apporter une vue d’ensemble de la production in vitro de plaquettes à partir de cellules iPS, et de son possible potentiel transformatif, d’importance capitale dans le domaine de la transfusion des produits sanguins.
Keywords: Bioreactors; Induced pluripotent stem cells; Megakaryocyte; Platelet transfusion.
© 2020 l'Académie nationale de médecine. Published by Elsevier Masson SAS. All rights reserved.
Figures
References
Publication types
LinkOut - more resources
Full Text Sources
Research Materials
