Plexiform Lesions in an Experimental Model of Monocrotalin-Induced Pulmonary Arterial Hypertension
- PMID: 33027370
- PMCID: PMC9363102
- DOI: 10.36660/abc.20190306
Plexiform Lesions in an Experimental Model of Monocrotalin-Induced Pulmonary Arterial Hypertension
Abstract
Background: The monocrotaline (MCT)-induced pulmonary arterial hypertension model is one of the most reproduced today, presenting as a limitation the absence of plexiform lesions, typical manifestations of the severe disease in humans.
Objective: To evaluate the severity of MCT-induced pulmonary arteriopathy by pathological findings of lung and heart tissue samples, clinical course and 37-day survival.
Methods: Fifty male Wistar rats were divided into one of the four groups - control (CG) (n = 10) and three intervention (MCT) groups. The MCT groups received intraperitoneal injection (60 mg/kg) of MCT and remained exposed to the substance for 15 days (G15, n = 10), 30 days (G30, n = 10) and 37 days (G37, n = 20). At the end of each period, the animals were sacrificed, and pulmonary and cardiac tissues were collected for anatomopathological and morphometric analysis. The Kruskal-Wallis test was used, considering a level of significance of 5%.
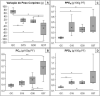
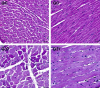
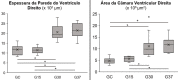
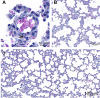
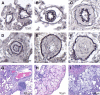
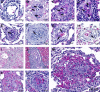
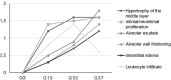
Results: In the lungs of MCT animals, lesions related to pulmonary arteriopathy were found, including muscularization of the arterioles, hypertrophy of the middle layer and concentric neointimal lesions. Complex lesions were observed in MCT groups, described as plexiform and plexiform-like lesions. Right ventricular hypertrophy was evidenced by increased thickness and diameter of the cardiomyocytes and a significant increase in the right ventricular wall thickness (p <0.0000).
Conclusion: The MCT model was able to generate moderate-severe pulmonary arteriopathy associated with secondary right ventricular hypertrophy. The 37-day survival rate was 50%. To our knowledge, this study was the first to note the presence of complex vascular lesions, similar to those observed in patients with severe pulmonary arterial hypertension, in an isolated MCT model. (Arq Bras Cardiol. 2020; 115(3):480-490).
Fundamento: O modelo de hipertensão arterial pulmonar induzida por monocrotalina (MCT) é um dos mais reproduzidos atualmente, apresentando como limitação a ausência de lesões plexiformes, manifestações típicas da doença grave em humanos.
Objetivo: Avaliar a gravidade da arteriopatia pulmonar induzida por MCT por meio dos achados anatomopatológicos pulmonares e cardíacos, evolução clínica e sobrevida em 37 dias.
Métodos: Foram utilizados 50 ratos machos Wistar divididos em quatro grupos, sendo um controle (n = 10). Os três grupos restantes foram submetidos à inoculação de MCT (60 mg/kg i.p.) e ficaram sob o seu efeito por 15 (n = 10), 30 (n = 10) e 37 dias (n = 20). Ao final de cada período, os animais foram sacrificados, obtendo-se tecidos pulmonar e cardíaco para análise anatomopatológica e morfométrica. Empregou-se o teste Kruskal-Wallis, considerando nível de significância de 5%.
Resultados: Nos pulmões dos animais MCT foram constatadas lesões referentes à arteriopatia pulmonar, incluindo muscularização das arteríolas, hipertrofia da camada média e lesões neointimais concêntricas. Lesões complexas foram observadas nos grupos MCT, descritas como plexiforme e do “tipo” plexiforme (plexiform-like). A hipertrofia do ventrículo direito foi constatada pelo aumento da espessura e diâmetro dos cardiomiócitos e pelo aumento significativo da espessura da parede do ventrículo direito (p<0,0000).
Conclusão: O modelo foi capaz de gerar arteriopatia pulmonar moderada-grave associada à hipertrofia do ventrículo direito secundária, com sobrevida de 50% em 37 dias. De nosso conhecimento, este estudo foi o primeiro a constatar a presença de lesões vasculares complexas, semelhantes às observadas em pacientes com hipertensão arterial pulmonar grave, em modelo isolado de MCT. (Arq Bras Cardiol. 2020; 115(3):480-490).
Conflict of interest statement
Potencial conflito de interesses
Declaro não haver conflito de interesses pertinentes.
Figures









Comment in
-
Plexiform Lesions in Pulmonary Arterial Hypertension: Are we Getting Closer to Manage with More Patience and Rigor?Arq Bras Cardiol. 2020 Sep;115(3):491-492. doi: 10.36660/abc.20200832. Arq Bras Cardiol. 2020. PMID: 33027371 Free PMC article. English, Portuguese. No abstract available.
References
-
- 3. Meyrick B. The Pathology of Pulmonary Artery Hypertension. Clin Chest Med. 2001;22(3):393-404. - PubMed
-
- 4. Heath D, Edwards J. The Pathology of Hypertensive Pulmonary Vascular Disease: A Description of Six Grades of Structural Changes in the Pulmonary Arteries with Special Reference to Congenital Cardiac Septal Defects. Circulation. 1958;18(4):533–47. - PubMed
-
- 5. Wagenvoort CA, Wagenvoort N. Pathology of Pulmonary Hypertension. New York: John Wiley & Sons;1977.
Publication types
MeSH terms
Substances
LinkOut - more resources
Full Text Sources
Medical

