El diálogo oculto entre el hueso y los tejidos a través del remodelado óseo
- PMID: 38634083
- PMCID: PMC11019877
- DOI: 10.1515/almed-2023-0101
El diálogo oculto entre el hueso y los tejidos a través del remodelado óseo
Abstract
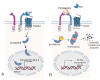
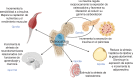
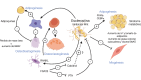
El hueso es mucho más que un reservorio de calcio y fósforo. Su disposición lacuno-canalicular ofrece una importante vía de intercambio con la circulación y actualmente, el esqueleto se considera un gran órgano endocrino, con acciones que van más allá del control del balance fosfocálcico mediado por el factor fibroblástico 23 (FGF23). Paralelamente al efecto modulador de las adipoquinas sobre el remodelado óseo, diversas proteínas óseas, como la osteocalcina y la esclerostina, ejercen cierta acción contra-reguladora sobre el metabolismo energético, posiblemente en un intento de asegurar los enormes requerimientos energéticos del remodelado. En esta interacción del hueso con otros tejidos, especialmente el adiposo, participa la señalización canónica Wnt/β-catenina y por ello la esclerostina, una proteína osteocítica que inhibe esta señalización, emerge como un potencial biomarcador. Es más, su participación en diversas patologías le posiciona como diana terapéutica, existiendo un anticuerpo anti-esclerostina, recientemente aprobado en nuestro país para el tratamiento de la osteoporosis. Esta revisión aborda el carácter endocrino del hueso, el papel de la osteocalcina y, especialmente, el papel regulador y modulador de la esclerostina sobre remodelado óseo y la homeóstasis energética a través de su interacción con la señalización canónica Wnt/β-catenina, así como su potencial utilidad como biomarcador.
Figures

References
LinkOut - more resources
Full Text Sources
